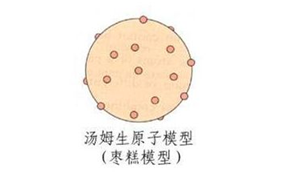
一、汤姆孙原子模型(”枣糕”模型)
(1)汤姆孙研究阴极射线用测定粒子比荷的方法发现了电子.电子的发现证明了原子是可分的.
(2)汤姆孙原子模型:原子里面带正电荷的物质均匀分布在整个原子球体中,而 带负电的电子则一粒粒镶嵌在球内.
二、卢瑟福:原子的核式结构
1.α粒子散射实验
(1)卢瑟福的α粒子散射实验装置(如下图所示)
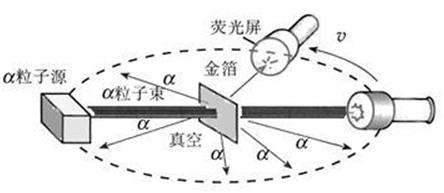
(2)α粒子散射实验现象:绝大多数α粒子穿过金箔后基本上仍沿原来的方向前进,少数α粒子穿过金箔后发生了大角度偏转,极少数α粒子甚至被反弹回来.
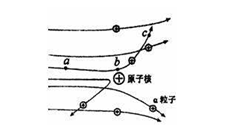
2.原子的核式结构
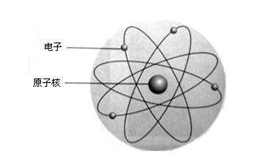
原子的核式结构模型:在原子中心有一个很小的核,原子全部的正电荷和几乎全部质量都集中在核里,带负电的电子在核外空间绕核旋转.
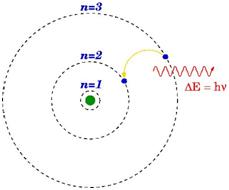
三、玻尔原子模型
1.模型
(1)轨道假设:原子中的电子在库仑引力的作用下,绕原子核做圆周运动,电子绕核运动的可能轨道是不连续的.
(2)定态假设:电子在不同的轨道上运动时,原子处于不同的状态,因而具有不同的能量,即原子的能量是不连续的.这些具有确定能量的稳定状态称为定态,在各个定态中,原子是稳定的,不向外辐射能量.
(3)跃迁假设:原子从一个能量状态向另一个能量状态跃迁时要吸收或放出一定频率的光子,光子的能量等于两个状态的 能级差,即hν=Em-En.
2.能级:在玻尔理论中,原子各个可能状态的能量值叫能级.
3.基态和激发态:原子能量最低的状态叫基态,其他能量(相对于基态)较高的状态叫激发态.
4.量子数:现代物理学认为原子的可能状态是不连续的,各状态可用正整数1,2,3,…表示,叫做量子数,一般用n表示.